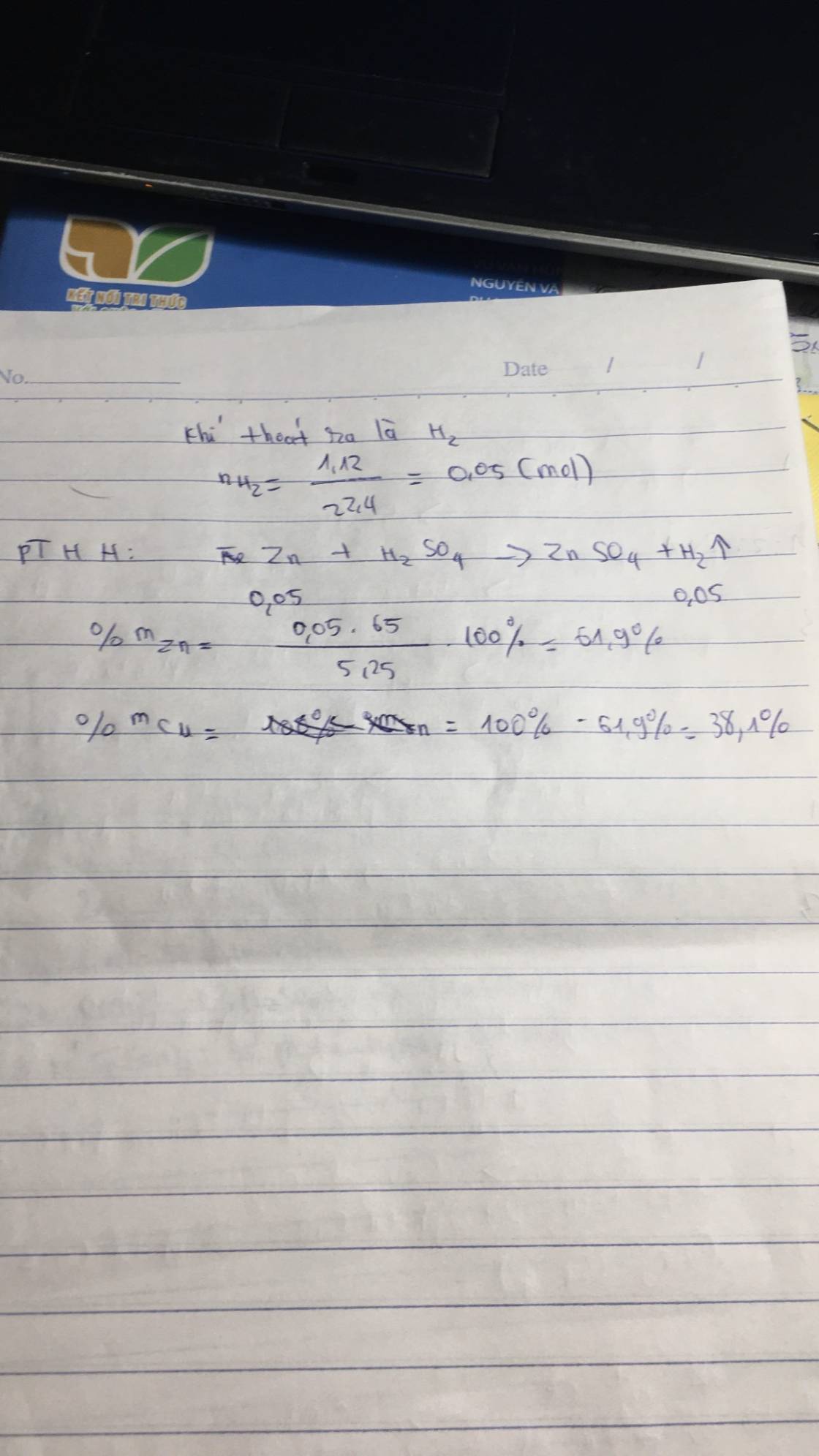Viết PTHH của phản ứng xảy ra ( nếu có ) khi lần lượt cho các kim loại : Zn , Al, Cu tác dụng với: a, O\(_2\) (t\(^o\)) ; b, Cl\(_2\) (t\(^o\)) ; c, Dung dịch \(H_2SO_4\) loãng ; d, Dung dịch FeSO\(_4\).

Những câu hỏi liên quan
viết PTHH của các phản ứng xảy ra ( nếu có ) khi lần lượt cho các kim loại: Zn, Al, Cu tác dụng với :
a)O\(_2\) (t\(^o\))
b) Cl\(_2\) (t\(^o\))
c) Dung dịch H\(_2\)SO\(_4\) loãng
d) Dung dịch FeSO\(_4\)
a)2Zn+O2--t0->2ZnO
2Al+3O2--t0->2Al2O3
b)Zn+Cl2--t0->ZnCl2
2Al+3Cl2--t0->2AlCl3
c)Zn+H2SO4--->ZnSO4+H2
2Al+3H2SO4--->Al2(SO4)3+3H2
d)2Al+3FeSO4--->Al2(SO4)3+3Fe
Zn+FeSO4--->ZnSO4+Fe
Đúng 0
Bình luận (2)
a, 2Zn + O2 -to--> 2ZnO
4 Al + 3O2 --to--> 2Al2O3
2Cu + O2 --to--> 2CuO
b, Zn + Cl2 ---> ZnCl2
2Al +3 Cl2 ---> 2AlCl3
Cu + Cl2 ---> CuCl2
c, Zn + H2SO4 → ZnSO4 + H2
Cu + H2SO4 → CuSO4 + H2
Al+ H2SO4 → Al2(SO4 ) 3+ H2
Đúng 0
Bình luận (0)
d, 2Al + 3 FeSO4 ---> Al2 (SO4)3 + 3Fe
Zn+FeSO4--->ZnSO4+Fe
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hoad tan 5,64g Culeft(NO_3right)_2 và 1,7g AgNO_3 vào nước được 101,43g dung dịch A. Cho 1,57g bột kim loại Al và Zn vào dung dịch A rồi khuấy đều. Sau khi các phản ứng xảy ra hoàn toàn thu được phần chất rắn B và dung dịch D chỉ chứa 2 muối. Ngâm B trong dung dịch H_2SO_4 loãng không thấy có khí thoát ra.
a,Viết các phương trình phản ứng xảy ra
b, Tính C% của mỗi muối trong dung dịch D
Đọc tiếp
Hoad tan 5,64g \(Cu\left(NO_3\right)_2\) và 1,7g \(AgNO_3\) vào nước được 101,43g dung dịch A. Cho 1,57g bột kim loại Al và Zn vào dung dịch A rồi khuấy đều. Sau khi các phản ứng xảy ra hoàn toàn thu được phần chất rắn B và dung dịch D chỉ chứa 2 muối. Ngâm B trong dung dịch \(H_2SO_4\) loãng không thấy có khí thoát ra.
a,Viết các phương trình phản ứng xảy ra
b, Tính C% của mỗi muối trong dung dịch D
Cho m gam hỗn hợp 2 kim loại Zn và Al tác dụng với dung dịch \(H_2SO_4\) loãng dư thu đc 10,08l khí (đktc) Mặt khác cho m gam trên tác dụng với dung dịch \(HNO_3\) đặc thì thu đc 20,16 l khí a) viết các PTHH xảy ra b) tính m
a) Zn + H2SO4 → ZnSO4 + H2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Zn + 4HNO3 → Zn(NO3)2 + 2NO2 + 2H2O
Al + 6HNO3→ Al(NO3)3 + 3NO2 + 3H2O
b) Gọi x,y lần lượt là số mol Al, Zn
\(\left\{{}\begin{matrix}x+\dfrac{3}{2}y=0,45\\2x+3y=0,9\end{matrix}\right.\)
=> Hệ PT vô số nghiệm, bạn xem lại đề nhé
Đúng 2
Bình luận (0)
Bài 3: Cho các oxit: K2O, CO, BaO, CO2, Al2O3, Fe3O4, và SiO2. Viết các PTPƯ xảy ra (nếu có) khi cho các oxit trên lần lượt tác dụng với H2O, dung dịch H2SO4 loãng và dung dịch KOH
Bài 4: Cho các kim loại Fe, Al, Cu lần lượt tác dụng với Cl2 và các dung dịch sau: ZnSO4, AgNO3, H2SO4, KOH. Viết các PTPƯ xảy ra (nếu có)
Bài 5: Cho các kim loại Cu, Al, Fe, Ag. Kim loại nào tác dụng được với dung dịch HCl, dung dịch CuSO4, dung dịch AgNO3, dung dịch NaOH? Viết các PTPƯ xảy ra
Đọc tiếp
Bài 3: Cho các oxit: K2O, CO, BaO, CO2, Al2O3, Fe3O4, và SiO2. Viết các PTPƯ xảy ra (nếu có) khi cho các oxit trên lần lượt tác dụng với H2O, dung dịch H2SO4 loãng và dung dịch KOH
Bài 4: Cho các kim loại Fe, Al, Cu lần lượt tác dụng với Cl2 và các dung dịch sau: ZnSO4, AgNO3, H2SO4, KOH. Viết các PTPƯ xảy ra (nếu có)
Bài 5: Cho các kim loại Cu, Al, Fe, Ag. Kim loại nào tác dụng được với dung dịch HCl, dung dịch CuSO4, dung dịch AgNO3, dung dịch NaOH? Viết các PTPƯ xảy ra
Bài 3
+ H2O
K2O+H2O---.2KOH
BaO+H2O--->Ba(OH)2
CO2+H2O--->H2CO3
+H2SO4 loãng
K2O+H2SO4--->K2SO4+H2O
BaO+H2SO4--->BaSO4+H2O
Al2O3+3H2SO4--->Al2(SO4)3+3H2O
+ dd KOH
CO2+2KOH--->K2CO3+H2O
CO2+KOH--->KHCO3
SiO2+2KOH--->K2SiO3+H2O
Bài 4Cho các kim loại Fe, Al, Cu lần lượt tác dụng với Cl2 và các dung dịch sau: ZnSO4, AgNO3, H2SO4, KOH. Viết các PTPƯ xảy ra (nếu có)
2Fe+3Cl2-->2FeCl3
2Al+3Cl2--->2AlCl3
Cu+Cl2---->CuCl2
+ và các dd sau là sao nhỉ..mk chưa hiểu ý đề bài
bài 5 Cho các kim loại Cu, Al, Fe, Ag. Kim loại nào tác dụng được với dung dịch HCl, dung dịch CuSO4, dung dịch AgNO3, dung dịch NaOH? Viết các PTPƯ xảy ra
+dd HCl
2Al+6HCl-->2AlCl3+3H2
Fe+2HCl---->FeCl2+H2
+dd CuSO4
2Al+3CuSO4--->3Cu+Al2(SO4)3
Fe+CuSO4--->Cu+FeSO4
+dd AgNO3
Cu+2AgNO3--->2Ag+Cu(NO3)2
Al+3AgNO3--->3Ag+Al(NO3)3
Fe+2AgNO3--->2Ag+Fe(NO3)2
+ dd NaOH
2NaOH+2Al+2H2O--->2NaAlO2+3H2
Bài 1; Chọn chất thích hợp để điền vào chỗ trống và cân bằng pthh:a) H_2 + O_2➞ ...b) N_2O_5 + H_2O➞ ...Bài 2: Cho 5,4 gam nhôm tác dụng vừa đủ với dung dịch axit sinfuric (H_2SO_4) loãng. Sau phản ứng thu đc nhôm saufat và khí hiđro.a) Viết pthh và tính kl của axit sunfuric (H_2SO_4) cấn dùng.b) Tính kl của nhôm sunfat tạo thành.c) Tính kl khí H_2 và thể tích khí H_2 sinh ra ở (đktc).Bài 3: Cho 8 gam 1 kim loại A (A có hóa trị x) tác dụng với nc dư thu đc 200ml dung dịch bazơ có nồng độ 1M. Hỏi...
Đọc tiếp
Bài 1; Chọn chất thích hợp để điền vào chỗ trống và cân bằng pthh:
a) H\(_2\) + O\(_2\)➞ ...
b) N\(_2\)O\(_5\) + H\(_2\)O➞ ...
Bài 2: Cho 5,4 gam nhôm tác dụng vừa đủ với dung dịch axit sinfuric (H\(_2\)SO\(_4\)) loãng. Sau phản ứng thu đc nhôm saufat và khí hiđro.
a) Viết pthh và tính kl của axit sunfuric (H\(_2\)SO\(_4\)) cấn dùng.
b) Tính kl của nhôm sunfat tạo thành.
c) Tính kl khí H\(_2\) và thể tích khí H\(_2\) sinh ra ở (đktc).
Bài 3: Cho 8 gam 1 kim loại A (A có hóa trị x) tác dụng với nc dư thu đc 200ml dung dịch bazơ có nồng độ 1M. Hỏi A là kim loại nào?
Bài 4; Gọi tên của các chất sau;
Fe\(_2\)(SO\(_3\))\(_3\), Mg(OH)\(_2\), H\(_3\)PO\(_3\), Ba(HSO\(_4\))\(_2\).
Bài 1:
H2 + O2 → H2O
N2O5 + H2O → HNO3
Bài 4:
Fe2(SO3)3: Sắt III sunfat
Mg(OH)2: Magie hidroxit
H3PO4: axit photphoric
Ba(HSO4)2: Bari Bisunfat
Đúng 3
Bình luận (0)
Bài 1 :
\(a.2H_2+O_2\underrightarrow{^{t^0}}2H_2O\)
\(b.N_2O_5+H_2O\rightarrow2HNO_3\)
Bài 2 :
\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(0.2............0.3...........0.1..............0.3\)
\(m_{H_2SO_4}=0.3\cdot98=29.4\left(g\right)\)
\(m_{Al_2\left(SO_4\right)_3}=0.1\cdot342=34.2\left(g\right)\)
\(m_{H_2}=0.3\cdot2=0.6\left(g\right)\)
\(V_{H_2}=0.3\cdot22.4=6.72\left(l\right)\)
Đúng 2
Bình luận (0)
Bài 3 :
\(n_{A\left(OH\right)_n}=0.2\cdot1=0.2\left(mol\right)\)
\(2A+2nH_2O\rightarrow2A\left(OH\right)_n+nH_2\)
\(0.2........................0.2\)
\(M_A=\dfrac{8}{0.2}=40\left(\dfrac{g}{mol}\right)\)
\(A:Canxi\:\)
Bài 4 :
Fe2(SO4)3 : Sắt (III) sunfat
Mg(OH)2 : Magie hidroxit
H3PO3: Axit photphoro
Ba(HSO4)2: Bari hidrosunfat
Đúng 2
Bình luận (0)
Cho kim loại Al lần lượt tác dụng với các chất: H2SO4 đặc nguội, dung dịch H2SO4 loãng, khí clo, dung dịch AgNO3 , dung dịch MgSO4 , dung dịch NaOH (các điều kiện phản ứng coi như có đủ). Số phản ứng hóa học xảy ra là:
A.3
B.4
C.6
D.5
Al + H2SO4 đặc nguội --> x
2Al + 3H2SO4 loãng --> Al2(SO4)3 + 3H2
2Al + 3Cl2 --to--> 2AlCl3
Al + 3AgNO3 --> Al(NO3)3 + 3Ag
Al + MgSO4 --> x
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
=> B
Đúng 2
Bình luận (0)
7. Một hỗn hợp X ở dạng bột gồm Cu và Zn. Để xác định phần trăm khối lượng của mỗi kim loại trong X, người ta lấy 5,25 gam X cho tác dụng với dung dịch \(H_2SO_4\) loãng dư thấy có 1,12 lít khí thoát ra (đktc).
Viết PTHH của phản ứng xảy ra và tính phần trăm khối lượng của mỗi kim loại trong hỗn hợp X ban đầu.
Cho 14,8g hỗn hợp Al, Fe và Cu vào lượng dư dung dịch H\(_2\)SO\(_4\). Sau phản ứng xảy ra hoàn toàn thu được 3,36 lít khí H\(_2\)(ĐKTC). Tính khối lượng mỗi kim loại trong hỗn hợp đầu.
Anh nghĩ đề đã thiếu khối lượng rắn sau phản ứng em nhé!
Đúng 0
Bình luận (0)
Cho a gam Al tác dụng vừa đủ với 100 gam dung dịch H_2SO_4. Sau phản ứng thất thoát ra 6,72 lít H_2 (ở đktc). Tính:
a) Giá trị a
b) Khối lượng muối tạo thành
c) Nồng độ phần trăm của dung dịch H_2SO_4 ban đầu
Đọc tiếp
Cho a gam Al tác dụng vừa đủ với 100 gam dung dịch H\(_2\)SO\(_4\). Sau phản ứng thất thoát ra 6,72 lít H\(_2\) (ở đktc). Tính:
a) Giá trị a
b) Khối lượng muối tạo thành
c) Nồng độ phần trăm của dung dịch H\(_2\)SO\(_4\) ban đầu
\(a)n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ 0,2\leftarrow-0,3\leftarrow-0,1\leftarrow---0,3\)
\(a=m_{Al}=0,2.27=5,4g\\ b)m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2g\\ c)C_{\%H_2SO_4}=\dfrac{0,3.98}{100}\cdot100=29,4\%\)
Đúng 2
Bình luận (0)
a)nH2=22,46,72=0,3mol2Al+3H2SO4→Al2(SO4)3+3H20,2←−0,3←−0,1←−−−0,3
Đúng 0
Bình luận (0)